发布日期:2021-08-17
点击量:
儿童呼吸性睡眠障碍(respiratorysleep disorders,RSD)的特征是上呼吸道不同程度的阻塞和夜间气体交换的不同程度改变。
第三版“国际睡眠障碍分类”(InternationalClassification of Sleep Disorders,ICSD-3)将OSAS定义为多导睡眠图(polysomnography,PSG)测定的阻塞性呼吸紊乱指数(respiratory disturbance index,RDI)≥5次/小时,与OSAS的典型症状(如睡不醒、日间嗜睡、疲劳或失眠、醒来有喘息感或鼾声、目击呼吸暂停)相关或RDI≥15次/小时(即使没有症状)。除了呼吸暂停和低通气指数(Apnea-Hypopnea Index,AHI)中包括的呼吸暂停和低通气外,RDI还包括呼吸暂停相关觉醒(respiratoryeffort-related arousals,RERA)。呼吸事件的评分在《AASM睡眠及相关事件评分手册:规则、术语和技术规范,2.3版》(AASM评分手册)中有定义。然而,应该注意到低通气事件定义中存在一些可变性。
根据AASM评分手册的推荐定义,血流变化应与3%的氧气饱和度降低和或皮质觉醒相关,但也可以接受另一种定义,即要求与4%的氧气饱和度降低相关,而不考虑皮质唤醒。根据使用的定义,任何给定个体的AHI可能有很大不同。这些定义与研究中使用的其他低通气定义之间的差异使得评估有关OSAS诊断的证据成为一件复杂的事情。
呼吸暂停低通气指数(apnea-hypopneaindex,AHI)是每小时呼吸紊乱事件的平均数。通常,阻塞性睡眠呼吸暂停综合征(obstructivesleep apnea syndrome,OSAS)被定义为AHI≥5。AHI为5-15被认为是轻度,15-30被认为是中度,每小时超过30次以上是重度睡眠呼吸暂停的特征。
成人OSAS的确切发病率尚不清楚。据估计,24%的男性和9%的女性有OSAS的呼吸症状,有或没有白天嗜睡,但大约80%的OSAS成人患者仍然没有得到诊断。
另一方面,儿童呼吸性睡眠障碍(respiratory sleep disorders ,RSD)的特点是上呼吸道不同程度的阻塞和夜间气体交换的不同程度的改变。
临床表现从习惯性打鼾到完全气道阻塞。欧洲呼吸学会(European Respiratory Society,ERS)儿童阻塞性RSD诊断和治疗工作组将OSAS定义为“一种睡眠期间上气道功能障碍的综合征,其特征是打鼾和/或继发于上气道阻力增加和咽部塌陷而导致呼吸频率增加”。在儿童OSAS患者中,临床表现的严重程度和日间症状之间没有明显的相关性,症状的范围更细微。
Gozal等人提出了诊断儿童OSAS的几个标准,分为主要标准和次要标准,最重要的是评估治疗的必要性。主要标准包括AHI>2、RDI>2、最低血氧饱和度(Nadir SpO2)<90%、日间嗜睡、学习障碍、多动行为、高血压、遗尿、肥胖。次要标准包括CRP、LDL、空腹胰岛素水平较高、HDL水平较低、复发性中耳炎和腺扁桃体分级>1。5项主要标准或3项主要标准加3项次要标准阳性,提示需要进行治疗。
根据最新的指南,儿童患者中OSAS的总体发病率约为2%。根据上呼吸道淋巴组织的相对大小,大多数儿童患者为2-8岁左右。OSAS在男性中比女性更常见。非裔美国人和肥胖儿童患OSAS的风险都在增加。尽管许多研究已经解决了成人OSAS的病因,但儿童患者中这种综合征的许多方面仍然不清楚。然而,有许多危险因素可以导致上呼吸道的缩窄或塌陷,这可能与OSAS的发病机制有关。
儿童OSAS的诊断包括详细的临床病史,重点是体检结果,尤其是耳鼻喉的体检结果,夜间和日间症状以及合并症,然后向父母发放特定的问卷。夜间血氧测定和动态多导睡眠监测是强制性的。对于术后残留的OSAS患者,应考虑DISE以检测潜在塌陷的解剖位置。
据我们所知,很少有文献发表与OSAS相关的危险因素,尤其是在儿童年龄。计算机检索Pubmed和MEDLINE网站2012-2019年的相关文章182篇,检索词为“危险因素;儿童OSAS;肥胖;腺体样肥大;颅面畸形;过敏性鼻炎;炎症”。只有123篇文章讨论了儿童的这一特定话题。另外,值得注意的是,大多数文献只分析了一个单一的危险因素,很少分析多个因素,主要集中在对OSAS的概述。MarcusC.L.等人和Li Z.等人发表的非常详尽的文献是这种观察性研究的典型例子。他们对病理学做了一个概括性的、精彩的陈述,但只用了几个段落来评估各种危险因素。
因此,本文的目的在于分析这方面的研究现状及其对诊断和治疗的影响。

在成人和儿童患者中,肥胖都是OSAS最重要的危险因素之一。
肥胖主要通过两种机制影响OSAS:咽部软组织水平的脂肪减少了管腔口径和增加结构本身的塌陷。其次,胸壁和腹壁脂肪含量的增加显著降低了这些患者的呼吸功能。
体重指数(body massindex,BMI)每超过50个百分位数,患OSAS的风险就会增加约10%。
从1975-2016年,全球儿童和青少年的平均BMI有所增加,2016年女孩达到18.6kg/m2(18.4-18.7),男孩达到18.5 kg/m2(18.3-18.7)。另外,儿童肥胖不仅是一种普遍现象,而且是一种持久的现象:大约50%的肥胖儿童也可能是肥胖成人。
与体重正常的儿童相比,超重或肥胖儿童患OSAS的风险更高。尽管腺扁桃体切除(adenotonsillectomy,AT)是这些儿童的一线治疗方法,但一些研究报告称肥胖会增加手术后持续性OSAS的风险。对此,Xu Z.等人提出了自己的看法。据报道,体重指数标准差得分(body massindex standard deviation score,BMI SDS)和AHI之间存在直接相关性。
减肥管理可能是治疗儿童和青少年肥胖相关OSAS的关键,尤其是对于那些既往进行过扁桃体切除但没有临床结果的患者。尽管许多研究支持将减肥管理作为肥胖成人OSAS的关键治疗方法,但只有少数研究了肥胖治疗对儿童OSA的影响。AndersenI.G.等人对在一家多学科慢性超重护理和肥胖治疗诊所接受治疗的62名儿童和青少年进行了一项前瞻性纵向研究。他们观察到,在肥胖治疗6个月后,38%的患者AHI恢复正常,在减肥一年后,44%的患者AHI恢复正常。
这些证据使我们考虑将减肥作为这些BMI升高儿童患者的一线治疗。
根据OSAS的高发年龄,Waldeyer环的淋巴组织在3-6岁之间较为发达。根据Friedman分级标准,腺样体和/或扁桃体肥大是儿童患者上气道管腔缩小的最常见原因(表1)。

表1:扁桃体大小临床分级的重复性研究。
扁桃体肥大导致腭后区变窄,该区横截面积最小,因此是最常见的梗阻部位,如图1中6岁患者所示。尤其是,患有IV级扁桃体(接吻扁桃体)的儿童患者非常容易发生睡眠障碍,原因是口咽狭窄和侧方塌陷。
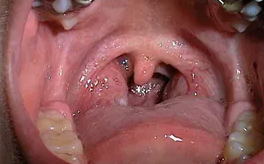
图1:1例6岁儿童Ⅲ级扁桃体肥大。
扁桃体肥大会导致经口呼吸、鼻塞、低鼻音、打鼾、慢性鼻窦炎和复发性中耳炎,以及大脑发育不良和情绪障碍。Kurnatowski P等人在他们对6到9岁儿童患者的研究中,与健康对照组相比,腺扁桃体肥大组的情绪不稳定得分较高,大多数儿童患者在术后3-10个月的行为表现良好。一些作者强调了炎症在扁桃体肥大和OSAS发展中的作用,考虑到扁桃体中各种炎症反应介质的表达增加,以及抗炎药物(如皮质类固醇)治疗后的改善,建议采取多学科的治疗方法。
外科治疗的金标准是腺扁桃体切除术。Brietzke等人展示了83%无其他合并症的OSAS儿童患者的多导睡眠图结果。最近的几项研究已经证实了这种疗效,但建议进行长期随访,尤其是对伴有合并症的儿童患者,以避免残留OSAS。另一方面,在OSAS成人患者中,扁桃体切除术更常与腭部手术相关。然而,Senchak AJ等人建议将扁桃体切除术作为单纯手术。他们招募了202名受试者。术前AHI为5.4-56.4次/小时。平均AHI从18次/小时降至3.2次/小时,减少了82%。单纯扁桃体切除术后,RDI中位数、Epworth嗜睡量表(Epworth Sleepiness Scale,ESS)和柏林评分均有统计学意义的降低。他们得出结论,成人患者单纯扁桃体切除术可能是有效的,尤其是对于扁桃体较大、中度OSAS和Friedman分期较低的年轻超重男性。
最近的研究也表明舌扁桃体肥大在儿童OSAS的发病机制中的作用,这在成人患者中已被证实。在成人患者中,通过经口腔机器人手术(Trans Oral Robotic Surgery,TORS)减少舌扁桃体的手术被广泛使用。在儿童患者中,这不是一种常见的手术。
在这类手术中,应该考虑使用廓清器或冷凝器行囊内扁桃体切除术的可能性,以便只切除扁桃体活跃的淋巴组织。据报道,与经典的囊外扁桃体切除术相比,类似的囊内扁桃体切除术似乎在降低AHI方面显示出相似的结果,术后出血的风险更低。
声门上成形术在喉软化伴丰富的杓状组织的病例中,或在会厌肥大/不稳定的病例中进行会厌成形术,都是可能的治疗选择,应始终考虑。
在儿童OSAS患者中,中线后舌切除术较少进行。
过敏性鼻炎(allergicrhinitis,AR)可能通过不同的机制影响睡眠。继发于鼻粘膜炎症过程的鼻塞会导致气道阻力增加,并可能导致经口呼吸、睡眠中断和疲劳。
鼻腔通畅主要受中、下鼻甲毛细血管的调节。过敏患者的症状是鼻阻力增加,这些毛细血管扩张、粘膜水肿和粘膜分泌。过敏性鼻炎患者最常见的症状是卡他、鼻塞或充血。显然,鼻塞也与嗅觉障碍有关,因为呼吸时进入鼻子的气味会减少。
气流速度的增加会进一步加剧气流受限,可能会导致鼻瓣和口咽部的反常气道狭窄,伴随阻塞的进展。
Lofaso等人使用后鼻压计强调鼻塞和OSAS严重程度之间的相关性,独立于其他危险因素。他们在两年的时间里评估了541名未经选择的连续打鼾患者 ,这些打鼾患者被怀疑在睡眠期间有呼吸障碍。另外,还获得了头部测量标志和体重指数(body mass index,BMI)。多导睡眠图被用来明确睡眠期间发生的异常呼吸事件的数量。他们得出结论,对鼻腔充血抑制剂无反应的永久性鼻塞和对鼻腔充血抑制剂有反应的功能性鼻塞(如血管舒缩性鼻炎期间发生的鼻塞)可能会导致睡眠呼吸障碍,并且是OSAS的独立危险因素。
McNicholas WT等人发现对豚草过敏的过敏性鼻炎患者出现阻塞性呼吸暂停的时间更长、频率更高,尤其是在豚草季节而不是花粉季节之后。另外,Mallampati评分升高似乎对这些患者有协同作用。
Liistro等人提出了一种二次打击的现象,与那些只有一个危险因素的人相比,那些由于舌根肥大和鼻塞而导致后咽空间缩小的人患OSA的相对风险更高。
另外,过敏过程中的炎性介质,如组胺和某些细胞因子,可能通过改变睡眠节律直接作用于中枢神经系统。最近在睡眠障碍的儿童患者中观察到,过敏性鼻炎(没有OSA)的存在会减少快速眼动(RapidEye Movement,REM)睡眠时间。Cao Y.等人最近的一项荟萃分析评估了成人和儿童患者中过敏性鼻炎与OSA之间的关系。他们纳入了44项研究,6086名参与者。他们报告称,在OSA/RSD患者中,被诊断为AR的儿童患者发病率是后者的2.12倍。然而,在成人患者中没有发现同样的趋势。可能的原因与儿童免疫系统不成熟有关。药物治疗,如鼻腔类固醇和口服孟鲁司特,已被研究为OSAS儿童患者伴发过敏性鼻炎和哮喘的一种治疗选择。Kheiranish-Gozal等人描述了在2-14岁的儿童患者中使用鼻内类固醇治疗和口服孟鲁司特的总体成功率为80%。该小组最近比较了口服孟鲁司特16周与安慰剂治疗儿童OSAS的效果,结果良好。
最近,美国儿科学会指出,鼻腔类固醇治疗适用于不能接受手术的轻度OSAS儿童患者或手术后持续残留OSAS的儿童患者。
颅面异常也可能是上呼吸道阻塞综合征的原因之一。下颌骨和舌头的大小、位置和几何形状的改变会导致腭后区增厚,如上所述,这是儿科患者最常见的梗阻部位。
遗传学在儿童OSAS发病机制中的确切作用仍存在争议。已知的是,一些临床症状,如唐氏综合征、威利综合征和伯-韦综合征,与OSAS密切相关。研究主要集中在基因多态性方面,如ApoE4等位基因、TNFa 308G基因多态性、NADPH基因多态性等。
Zaffnello M.等人报道了其他可能导致OSAS的遗传综合征:软骨发育不全、埃勒斯-丹洛斯综合征、皮埃尔·罗宾序列/复合体、埃利斯-范·克里夫德综合征、镰刀细胞病和努南综合征。任何涉及呼吸控制中心的先天或后天疾病都可能导致OSAS的发生。脊髓脊膜膨出、先天性小脑延髓下疝畸形以及外伤、肿瘤、手术造成的脑损伤可能是儿童患者的其他原因。在这类患者中,手术治疗往往是唯一可能的选择。双颌前移术(Maxillo-mandibular advancement,MMA)是此类病例中最常用的手术方式之一。它通过推进软腭和舌头并缩小咽侧壁来扩大鼻咽、口咽和下咽。
Saxby等人评价双颌前移术是治疗儿童综合征性颅面畸形的金标准。该手术显示,65名患者中的大多数患者的呼吸暂停低通气指数评分和OSA分级都有改善,尽管氧合测量没有显示出差异。
另一方面,在成人患者中,中面部前移的适应证应该考虑并发症发生率和成形手术后遗症。出于这个原因,它不被认为是没有面部畸形的儿童患者的第一线选择。
对于易患OSAS的患者,正畸治疗是一种有效的替代治疗方法,仅适用于出现高弓形或窄腭的患者。在最近的一项荟萃分析中,使用快速上颌骨扩张术(一种用于加宽腭部和扁平腭弓的器械)可以改善多导睡眠图结果。Villa等人建议将口腔矫治器用于治疗出现中到重度OSAS伴咬牙错合的儿童患者。
目前认为炎症与OSAS密切相关。事实上,OSAS患者全身炎症标志物如NF-κB、C-反应蛋白(CRP)、TNF-α、IL-6、IL-8、IL-1α、IL-1β和IFN-γ水平均上调。另一方面,伴随而来的抗炎因子IL-10的降低提示OSAS患者处于促炎状态。
一些研究强调了氧化应激在成人和儿童OSAS患者内皮损伤发生中的作用。间歇性低氧血症导致缺氧和再氧合,从而触发氧自由基的产生,从而引发局部和全身炎症。
许多研究表明NF-κB相关的炎症通路参与了OSAS的发病过程。NF-κB的上调增加了促炎介质和细胞因子(TNF-α、IL-6和CRP)的表达,导致血管内皮损伤和全身炎症。人们普遍认为,在成人患者中,全身炎症与动脉粥样硬化和冠状动脉疾病的进展之间存在相关性。
尽管在成人患者中炎症和OSA之间的联系是众所周知的,但在儿童患者中这一联系仍在争论中。在儿童患者中,炎症标志物(局部和全身)和促炎细胞因子上调,从而进一步促进淋巴组织的增殖。基于高水平的促炎因子,许多关于使用生物标志物诊断OSAS的研究正在进行中。
生物标志物是一种非侵入性、简单的综合诊断方法。激肽释放酶-1、类粘蛋白-1、尿调蛋白和尿辅酶-3是最常用的药物。事实上,它们的相关性在于找到OSAS检查的儿童患者的诊断精度。其他较少使用的生物标志物有:血清α淀粉酶水平、载脂蛋白型前列腺素D合成酶、半胱氨酰白三烯和尿8-异前列腺素。尽管结果似乎很有希望,但不幸的是,这些测试显示出不可靠的特异性和敏感性。事实上,慢性炎症可能是典型的OSAS患者(包括成人和儿童患者),也可能在以后发展。因此,生物标志物不能作为预测指标。因此,内科医生只应将其视为来自临床评估和PSG的数据的整合。
儿童OSAS的临床表现很有启发性,可分为躯体表现和症状。在一般检查中,这些患者表现为肥胖、长脸综合征、头面部改变和全身血压升高。另外,耳鼻喉查体可能常表现为扁桃体肥大、鼻黏膜发炎、鼻中隔偏曲、下鼻甲肥大、卵圆腭或巨舌症。
典型的症状可分为夜间症状和日间症状。在后者中,最常见的是日间嗜睡、反复头痛、鼻语、多动、注意力不集中、抑郁、情绪不稳定、易怒和攻击性。夜间症状包括打鼾、目击呼吸暂停、经口呼吸、反常的胸部运动、噩梦、梦游和夜间遗尿。
成人患者中众所周知的长期并发症也应该被提及,因为它们也可能发生在OSAS的儿童患者中。事实上,几项研究表明,患者心血管和肺部并发症的风险增加,如肺动脉高压、肺心病和右心衰竭。的确,OSAS儿童患者的CRP、脑钠素、黏附分子、骨髓样相关蛋白8/14、脂肪酸结合蛋白以及其他由血管损伤和内皮激活引起的因素都被证明是高水平的。
另外,患有严重OSAS的儿童患者可能发展为早期代谢综合征。这种危重情况的特点是一系列的病理改变:肥胖、胰岛素抵抗、全身性高血压和血脂异常。尽管这种联系尚不清楚,但几项研究已经强调了肥胖儿童患者的睡眠片断和间歇性缺氧以及胰岛素敏感性下调之间的联系。
儿童OSAS的诊断是一个由几个步骤组成的过程。儿童患者的临床表现更为微妙,因此简单的临床评估往往具有误导性。疑似OSAS患者的临床病史通过向其父母发放特定问卷来重建。调查问卷的作用及其在诊断过程中的有效性目前正在研究中。尤其是,在所有已开发的药物中,有6种是最有趣的,也是在临床实践中使用最频繁的。
儿科睡眠问卷(PediatricSleep Questionnair,PSQ)是使用最广泛的调查,由22个封闭式问题组成。
欧洲呼吸学会特别工作组目前的指南将PSQ定义为一种很好的测试,用于识别AHI>5、受OSAS困扰的儿童患者。
其他不太常用的问卷还有:睡眠临床记录(Sleep clinical record,SCR)、OSA-18、Broullette评分(Broullette score,BS)和我困了(I’M SLEEPY)。
最新的一份是《无眠睡眠干扰休息问卷》(Sleeping Sleepless Sleepy Disturbed Rest questionnaire,SSSDR)。它于2018年在罗马提出,没有包括在最新的指导方针中,但似乎非常有希望。
Burghard等人对这些问卷进行了汇总。尽管非常有用,但它们仍然需要更多的研究来改进或需要进一步的诊断步骤。在评估病史和问卷后,一般检查和耳鼻喉检查是首要的。一般查体评估以下参数:身高和体重增长、神经行为因素、心脏病和肺部疾病,以及最终的合并症。因此,几位专家之间的合作似乎是至关重要的。耳鼻喉体检包括对上呼吸道的准确评估。腺样体肥大通过鼻内镜进行评估。关于单纯腺样体肥大在OSAS的发生中可能起到的作用,存在着相互矛盾的观点。事实上,许多研究表明,腺样体肥大并不足以明确OSAS,但在有其他危险因素的儿童患者中,腺样体肥大会加重其严重程度。如前所述,扁桃体肥大是其他健康儿童OSAS最常见的原因之一,扁桃体分级与OSAS严重程度也有相关性。
然而,并不是所有有明显扁桃体肥大的儿童都会受OSAS影响。因此,上气道肌张力存在个体差异。尤其是在肥胖儿童患者和那些患有神经肌肉疾病的儿童患者中,扁桃体肥大并不起重要作用。
颌面畸形的存在也属于OSAS儿童患者的典型表现。因此,耳鼻喉专科医生也应该让口腔科正畸医生参与进来,通过评估口腔内外的形态学特征,选择适合保守治疗的患者。然而,最近的研究表明,扁桃体切除术能够恢复正确的上颌骨形态,从而支持颌面部骨骼异常更多地是OSA的结果而不是原因的观点。
夜间血氧饱和度是临床上怀疑儿童出现OSAS最广泛使用的筛查技术。事实上,它的成本很低,而且很容易执行和解读。尽管它的阳性结果可以诊断为OSAS,但它的阴性结果并不能排除OSAS。根据Kirk等人的观点,与实验室PSG相比,血氧饱和度测定对中度OSAS(AHI>5/h)诊断的敏感性和特异性分别为67%和60%。这些作者还注意到,血氧测定法在低水平时倾向于高估ODI,而在高水平时倾向于低估ODI。因此,仅靠血氧测定不足以诊断OSAS。
动态多导睡眠图是在患者家中对睡眠期间的心肺功能进行监测。尽管这种检查在成人患者身上进行的敏感性和特异性很高,但它在儿童患者中的有效性与他们的年龄密切相关。事实上,尽管有几项研究证实了它在学龄儿童中的有效性,但关于年龄较小的儿童的数据存在一些差异。Zucconi等人提出了一种家用便携式系统,包括测量气流、打鼾、胸壁和腹壁运动、心电图(ECG)、体位和血氧计。他们在睡眠实验室里用它进行研究。对12名3-6岁的儿童患者进行了常规的PSG检查,并在实验室内连续几晚使用便携式系统进行便携式测试。结果显示,检测呼吸窘迫指数有较好的敏感性,但特异性较差。
夜间实验室多导睡眠监测被认为是高度怀疑患有OSAS的儿童患者的金标准。它可以对睡眠期间的脑电图以及心肺功能、气流和夜间血氧仪进行监测。它可用于量化疾病的严重程度、术前评估、预测术后并发症和治疗后睡眠呼吸障碍的持续性。一个重要的方面是,儿童患者和成人患者对这项考试的遵守程度是不同的。事实上,成人患者中有一种焦虑的成分,使患者得不到充足的睡眠。同样的情况不会发生在儿童患者身上。这在几项研究中得到了很好的解释,这些研究评估了所谓的夜间变异性,最终得出的结果是,对儿童患者来说,一晚的PSG就足够了。
还有另一种用于儿童患者的测试:午睡睡眠诱发电位(Nap PSG)。它记录了白天实验室条件下的睡眠和呼吸情况。这是一种简单可靠的检测方法,具有较高的敏感性和特异性。
药物诱导睡眠内镜(Drug-inducedsleep endoscopy,DISE)主要用于儿童患者,以正确处理术后残留OSAS的儿童患者。主要目的是分析潜在塌陷解剖部位的梗阻类型
麻醉方案代表了一个有争议的观点。最初使用氟烷或七氟醚吸入治疗,但咽肌张力的几次改变导致它逐渐被静脉药物取代,如异丙酚、氯胺酮与甘氨蝶呤、瑞芬太尼和咪达唑仑。
Chen等人评估了DISE在儿童患者小扁桃体的诊断和针对性治疗中的作用。他们的结论是,DISE还需要评估在临床检查中发现小扁桃体的患者联合行腺扁桃体切除术的必要性。他们将重点放在清醒内镜检查和DISE检查之间的区别上。主要原因是可能低估了清醒状态崩溃的可能性。另外,DISE对口咽部梗阻的明确程度优于清醒内镜检查。
总而言之,尽管DISE在成人患者中有明确的编纂,但对儿童患者就不是这样了。考虑到文献中发表的第一项关于睡眠内镜检查的研究是Croft于1990年在儿童患者中进行的研究,这可以被认为是一个悖论。
儿童OSA是一种由多种因素引起的疾病。因此,研究每个单独的危险因素以及相关的合并症,以及对患者的持续监测是至关重要的,以便能够正确地计划并最终修改治疗过程。


